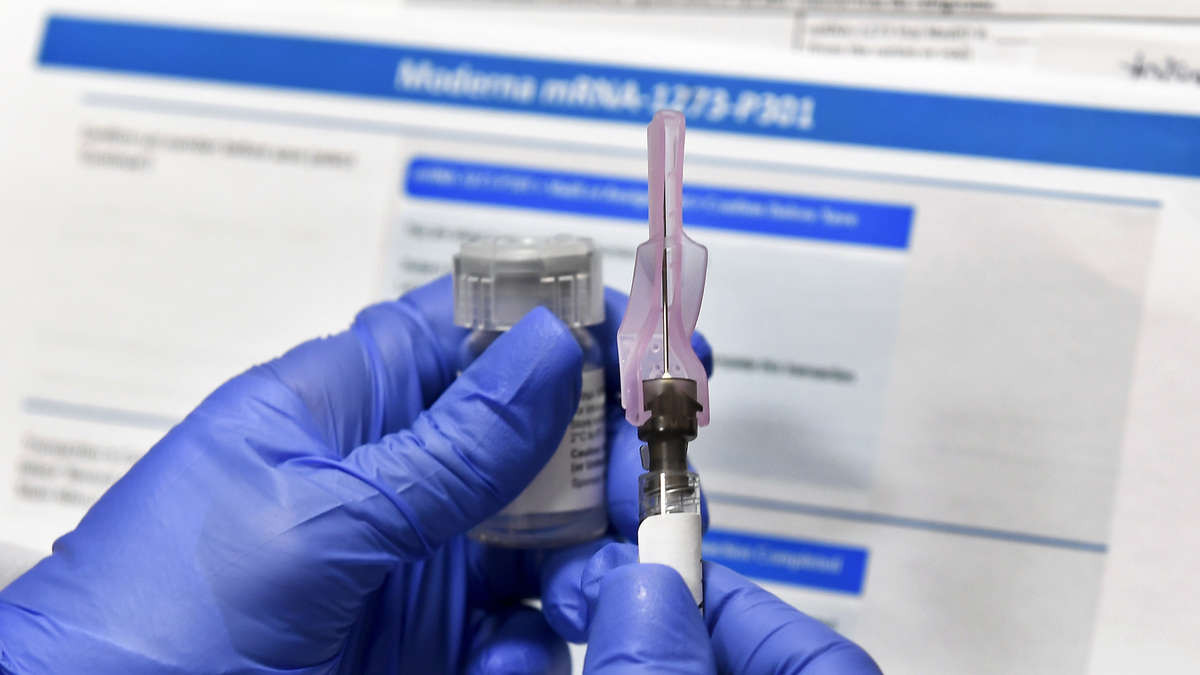
Corona-Impfstoff: Moderna will heute in Europa die Zulassung beantragen
-
vonPatrick Huljina
daraus schließen
Das US-amerikanische Pharmaunternehmen Moderna will am Montag die Zulassung seines Corona-Impfstoffs in der EU beantragen. Gleichzeitig muss in den USA eine Notfalllizenz beantragt werden.
- Amerikanisches Pharmaunternehmen Modern hat ein Impfstoff gegen das Coronavirus * entwickelt.
- Montag will das Unternehmen Eintritt in dem ich Anfrage.
- das Corona-Impfstoff * hat laut Moderna eine Wirkungsgrad von 94,1%.
New York – Das amerikanische Pharmaunternehmen Modern will das erste Unternehmen sein Zulassung eines Corona-Impfstoffs in dem ich Anfrage. Der Antrag auf bedingte Zulassung wird voraussichtlich am Montag bei der Europäischen Arzneimittel-Agentur EMA eingereicht, teilte das Unternehmen mit. Parallel dazu a Notfallgenehmigung mit der United States Medicines Agency FDA gefragt werden.
Corona-Impfstoff: Moderna will die Zulassung in Europa beantragen
Mit dem Antrag auf Genehmigung durch die EMA a Gekrönt *-Impfung auch in Deutschland näher. Letzte Woche hat der Leiter der Europäischen Kommission Ursula von der Leyen kommuniziert mit Modern ist eine Rahmenvereinbarung für Bis zu 160 Millionen Impfstoffdosen wurde beendet. Daher müssen zunächst 80 Millionen Dosen geliefert werden, mit der Option auf weitere 80 Millionen Einheiten. In der EU laut Moderna schon im dezember geliefert, sofern es genehmigt ist.
Wir haben gerade die primäre Wirksamkeitsanalyse in der Phase-3-COVE-Studie für mRNA-1273, unseren COVID-19-Impfstoffkandidaten, angekündigt und planen heute, eine Genehmigung für die Verwendung von zu beantragen Notfall von der US FDA und bedingte Genehmigung von der EMA. Weiterlesen: https://t.co/90FbcVHdWN pic.twitter.com/36tpY0QeFl
– Modern (@moderna_tx) 30. November 2020
Damit Corona-Impfstoff * von Modern Bei der EMA ist bereits ein sogenanntes in Arbeit Kontinuierlicher Überprüfungsprozess, was den Genehmigungsprozess beschleunigen soll. Hersteller können bereits vor dem vollständigen Zulassungsantrag individuelle Unterlagen zur Qualität, Sicherheit und Wirksamkeit einer Zubereitung einreichen.
Moderna Corona-Impfstoff: 94,1% wirksam
das Moderna-Impfstoff mRNA-1273 hat ein Wirkungsgrad von 94,1%wie das Unternehmen angekündigt. Dies geht aus der letzten Datenanalyse hervor klinische Phase-III-Studie von 30.000 Menschen in der Vereinigte Staaten teilnehmen. Die Hälfte der Teilnehmer erhält den Impfstoff, die andere Hälfte ein Placebo. Für einen vollständigen Impfschutz sind in Intervallen zwei Dosen erforderlich.
Alles in allem gehörten sie also bisher zu den Themen 196 Fälle Krankheit Covid19 * genehmigt. 11 dieser Fälle betrafen die Impfstoffgruppe und 185 die Placebogruppe. Daraus kann berechnet werden Wirkungsgrad von 94,1%. Die neuen Ergebnisse entsprechen in etwa den vorläufigen Daten, die Modern Veröffentlicht Mitte November. Das Unternehmen gab auch bekannt, dass die Summe 30 schwere Kurse von Covid-19 in der Studie nur die Placebogruppe besorgt. das Effizienz mRNA-1273 war laut Moderna in allen Altersgruppen ähnlich. (ph / dpa) * Merkur.de ist Teil des Ippen-Digital-Verlagsnetzwerks

Hardcore-Musikfanatiker. Food-Evangelist. Freiberuflicher Spieler. Wannabe-Schriftsteller. Wegbereiter der Popkultur. Lebenslanger Unternehmer. Reise-Guru.

