Kann ein Schachgroßmeister die Welt retten?

Er wurde 1986 in Albanien (Tirana) geboren. Seine Eltern zogen mit sechs Jahren nach Italien und er wurde 2007 italienischer Staatsbürger.
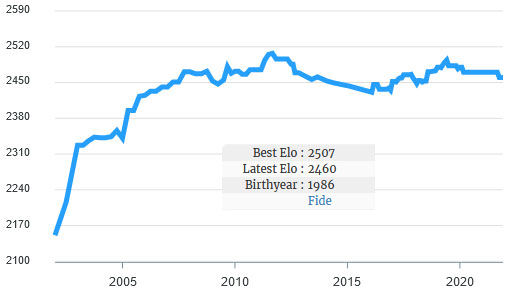
Luca (wie ihn seine Freunde nennen) ist ein sehr starker Spieler, der 2003 die albanische Schachmeisterschaft gewann und Albanien zweimal bei den Olympiaden (Calvia 2004 und Turin 2006) und Italien einmal bei den Olympiaden (Dresden 2008 – Bild oben, von Cathy) vertrat Rogers, wurde dort mitgenommen) und einmal bei einer Team-Europameisterschaft (Novi Sad 2009).
Er gewann die albanische Meisterschaft (2003), die italienische Schnellschachmeisterschaft (2009), und die italienische Tag-Team-Meisterschaft 2016 für das Team Fischer Chieti.
Luca wurde der Titel im Oktober 2018 verliehen, der 14. italienische Spieler, der den GM-Titel gewann.
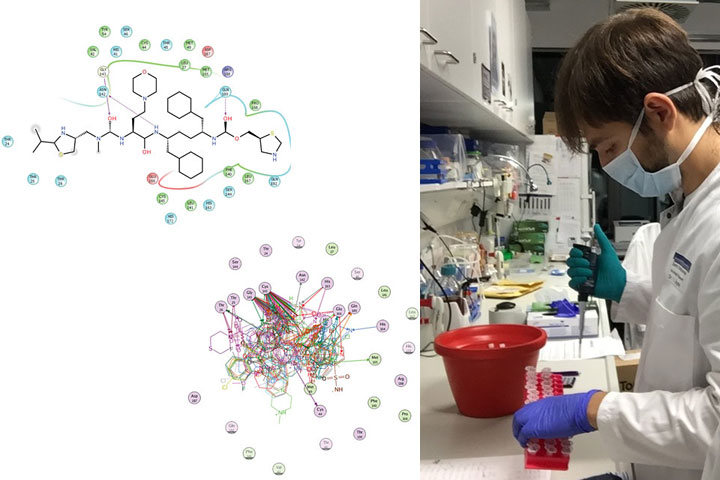
Im wissenschaftlichen Bereich hat Luca einen Master-Abschluss in Genetik und Molekularbiologie (von der Universität “La Sapienza” in Rom). Er promovierte in „Medizinische Mikrobiologie, Immunologie und Infektionskrankheiten“ und arbeitete an einem HIV-Heilungsprojekt unter der Leitung von Andrea Savarino. Später forschte er am Italian Institute of Health in Rom und an der Universität Heidelberg in Deutschland. Derzeit ist er Gastprofessor an der Federal University of Sao Paulo in Brasilien.
Als ich Luca den Click-Bait-Titel meines Artikels zeigte, fragte er mich, ob ich das Betteridge-Gesetz kenne, das besagt, dass „jeder Titel, der mit einem Fragezeichen endet, mit dem Wort nein beantwortet werden kann“. Ich hoffe sehr, dass das hier nicht der Fall ist. Ich drängte Luca, seine Versuche, die kleinen Holzstücke auf einem Schachbrett etwas besser als die anderen neu anzuordnen, aufzugeben und sich auf die dringendsten globalen Aufgaben zu konzentrieren, die es zu lösen gilt.
Cobicistat
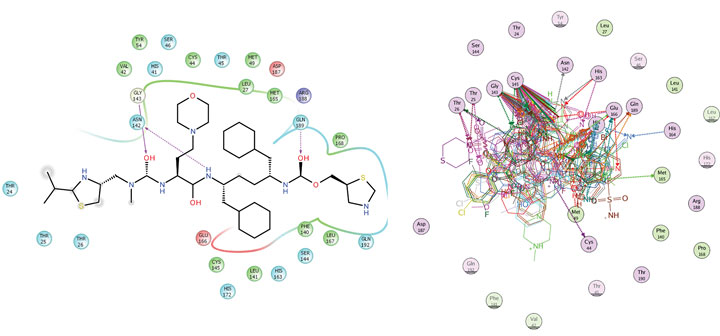
Luca und sein Team arbeiteten an Cobicistat, einem Medikament zur Behandlung von HIV/AIDS, das zeigte, dass es eine Wirkung gegen COVID-19 haben könnte. Das ist das Ergebnis einer bisher nur in vitro und am Tiermodell durchgeführten Studie, die im Journal der American Society of Microbiology, mBio, veröffentlicht wurde.
Das hat das internationale Autorenteam bewiesen Cobicistat hemmt die Replikation von SARS-CoV-2 mit einem anderen Mechanismus als derzeit verwendete Medikamente, nämlich durch Blockieren der Fusion des Virus mit seinen Zielzellen. Darüber hinaus kann das Medikament das Fortschreiten der Krankheit in einem Hamster-Tiermodell (Mesocricetus auratus) abschwächen, indem es die Wirkung eines anderen zuvor gegen COVID getesteten Medikaments, nämlich Remdesivir, verstärkt.
Wenn Sie an den Details der Forschung interessiert sind, ist der Artikel über COVID jetzt veröffentlicht und kostenlos zu lesen:
Abstrakt
Kombinationen von direkt wirkenden Virostatika werden benötigt, um Arzneimittelresistenzmutationen zu minimieren und die Replikation von RNA-Viren stabil zu unterdrücken.
Derzeit gibt es nur begrenzte Behandlungsmöglichkeiten für das schwere akute respiratorische Syndrom Coronavirus 2 (SARS-CoV-2), und die Prüfung einer Reihe von Behandlungsschemata hat zu widersprüchlichen Ergebnissen geführt.
Hier zeigen wir, dass Cobicistat, ein von der FDA zugelassener Wirkstoffverstärker, der die Aktivität von Cytochrom P450-3As (CYP3As) und P-Glykoprotein (P-gp) blockiert, die Replikation von SARS-CoV-2 hemmt. Zwei unabhängige Zell-zu-Zell-Membranfusionsassays zeigten, dass die antivirale Wirkung von Cobicistat durch die Hemmung der Spike-Protein-vermittelten Membranfusion vermittelt wird. Dementsprechend verringerte die Inkubation mit Cobicistat in niedrigen mikromolaren Konzentrationen die virale Replikation in drei verschiedenen Zelllinien, einschließlich Zellen pulmonalen und intestinalen Ursprungs.
Bei Anwendung von Cobicistat in Kombination mit Remdesivir wurde in Zelllinien und in einem primären Organoid des menschlichen Dickdarms eine synergistische Wirkung auf die Hemmung der Virusreplikation beobachtet. Dies stand im Einklang mit den Wirkungen von Cobicistat auf zwei seiner bekannten Targets, CYP3A4 und P-gp, deren Stummschaltung die antivirale In-vitro-Aktivität von Remdesivir in der Art von Cobicistat stimulierte.
Bei In-vivo-Verabreichung an Syrische Hamster in hohen Dosen senkt Cobicistat die Viruslast und dämpft das klinische Fortschreiten. Diese Daten unterstreichen Cobicistat als therapeutischen Kandidaten für die Behandlung der SARS-CoV-2-Infektion und als potenziellen Baustein von Kombinationstherapien für COVID-19.