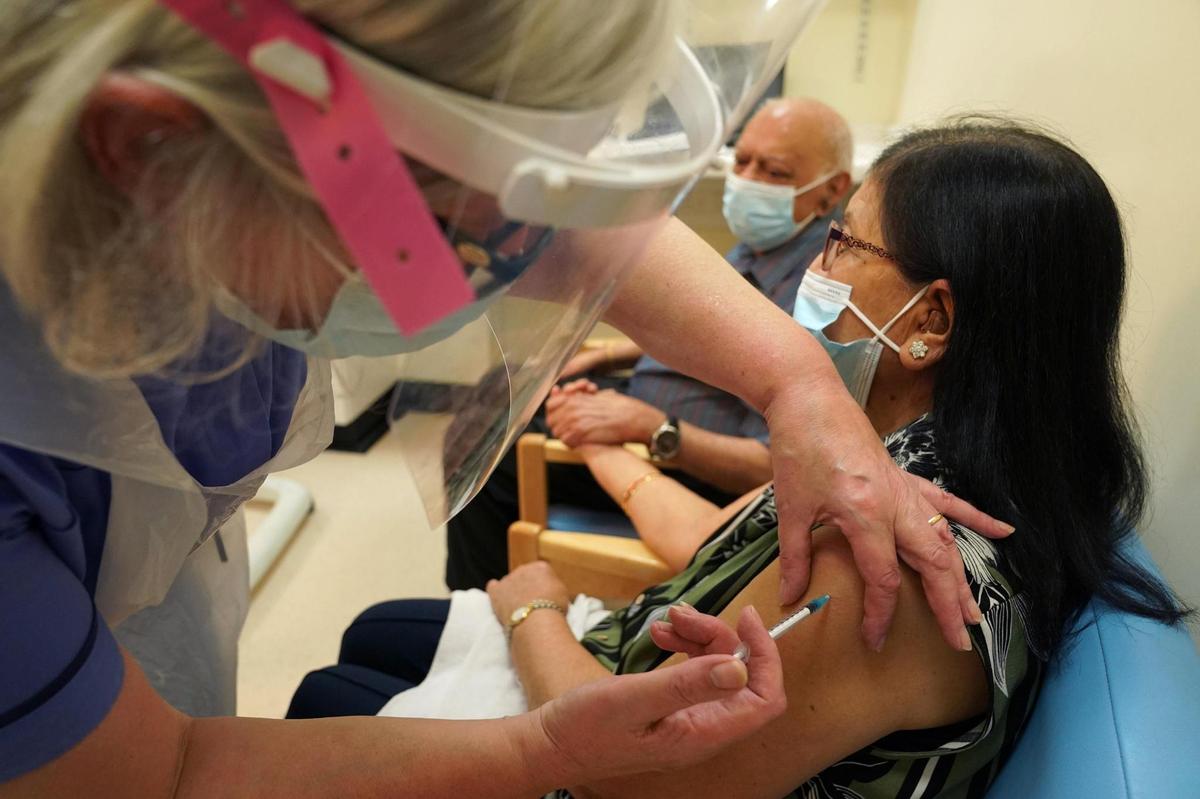
Wie die Studien durchgeführt werden – Ist es ethisch vertretbar, einen wirksamen Impfstoff für Probanden beizubehalten?
Hersteller möchten Langzeiteffekte untersuchen oder neue Impfstoffe testen. Die Zulassung wirksamer Impfstoffe stellt sie vor neue Herausforderungen.
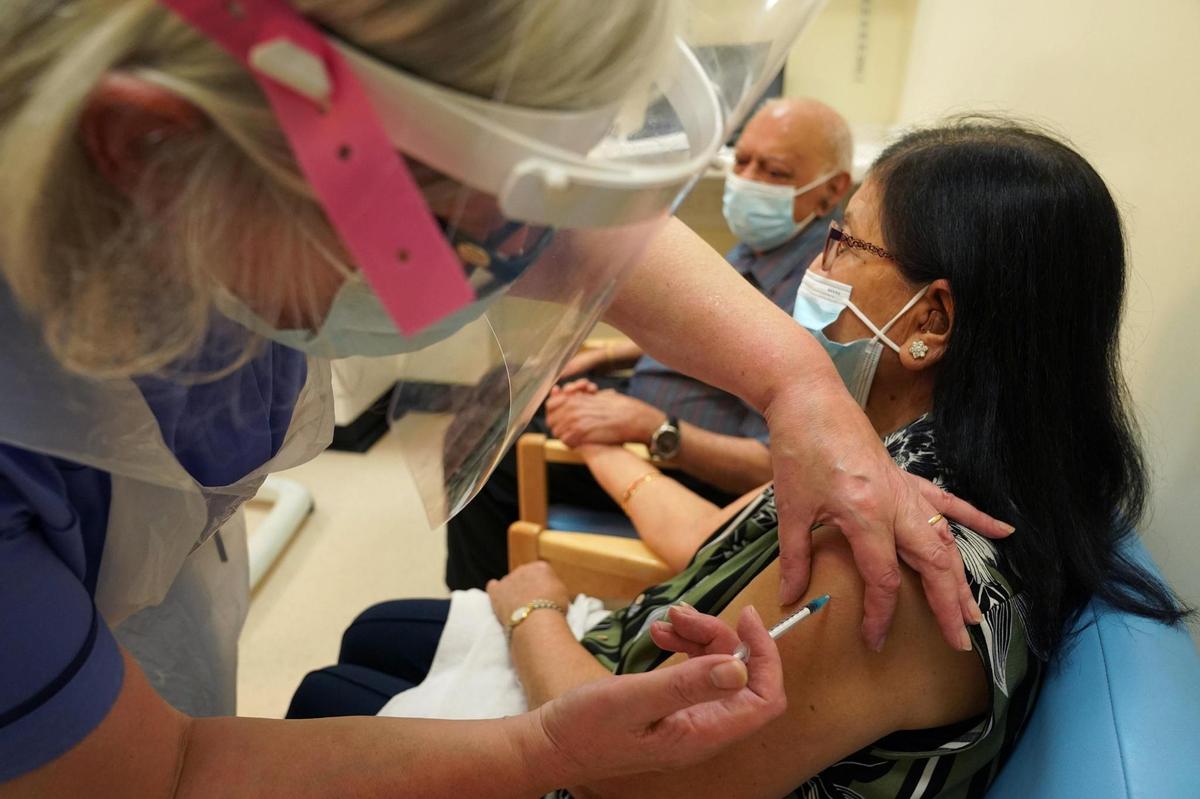
Die Briten sind bereits geimpft. Für andere Studien sollten die Testpersonen jedoch anstelle des geeigneten Impfstoffs auch ein Placebo erhalten. Ihre Gesundheit bleibt in Gefahr, auch wenn bereits wirksame Mittel vorhanden sind.
Foto: Owen Humphreys (Getty Images)
Die ersten Personen werden außerhalb klinischer Studien gegen das Coronavirus geimpft. Weltweit sind noch viele andere Impfstoffe im Umlauf. Was bedeuten die ersten Zulassungen für die weitere Impfstoffentwicklung?
In den letzten Wochen haben drei Hersteller von Coronavirus-Impfstoffkandidaten vielversprechende Daten veröffentlicht. In der Schweiz werden voraussichtlich Anfang nächsten Jahres die ersten Menschen geimpft. So gut die Nachrichten auch sind, es stellt die Impfstoffentwicklung vor Herausforderungen.
In der medizinischen Forschung ist es üblich, dass die Hälfte der Studienteilnehmer den Wirkstoff und die andere Hälfte ein Placebo erhält. Auf diese Weise kann die Wirksamkeit und Sicherheit des Impfstoffs überprüft werden. Aber ist es ethisch vertretbar, Placebo-Patienten nach der Zulassung einen wirksamen Impfstoff zu verweigern, um die Langzeiteffekte zu untersuchen?
Eine „Grauzone“
Dies sind Fragen, denen wir uns vor der Koronapandemie selten stellen mussten, sagte die Medizinethikerin Samia Hurst von der Universität Genf in einem Interview mit der Nachrichtenagentur Keystone-SDA. Eine „Grauzone“ öffnet sich mit beispielloser Geschwindigkeit.
Was sie damit meint: Sobald ein Impfstoff als Standard der Gesundheitsversorgung anerkannt ist, müssen Placebo-Teilnehmer auch den wirksamen Impfstoff erhalten.
Aber solange Impfstoffe knapp sind und bestimmten Personengruppen Vorrang eingeräumt wird, wird bestimmten Personen nichts verweigert, sagte Hurst. „Während dieser Zeit kann es ethisch vertretbar sein, bestimmten Testpersonen weiterhin Placebos zu verabreichen.“
Langzeitfolgen können ohne Placebogruppen kontrolliert werden
Und was passiert, nachdem alle Studienteilnehmer geimpft wurden? „Sie können die Langzeitfolgen ohne Placebogruppen untersuchen“, sagte der Epidemiologe Marcel Tanner von der wissenschaftlichen Task Force. Mit dem Impfprotokoll können Sie jederzeit bestimmen, welche Nebenwirkungen bei geimpften Personen und welche bei nicht geimpften Personen auftreten würden.
Aber: „Dieses Verfahren dauert länger als kontrollierte Studien“, sagte Hurst. Da die Gruppen nicht mehr zufällig ausgewählt werden, ist das Datenrauschen wichtiger.
Weitere Prüfung in Phase 4
Die Impfstoffüberwachung endet nicht mit der Genehmigung. Während der Phase 4 sollte die routinemäßige Anwendung überprüft werden, um festzustellen, ob eine asymptomatische Infektion vermieden werden kann und ob geimpfte Personen das Virus weiterhin übertragen können, sagte Tanner.
Abhängig von den Daten aus den Phase-3-Studien werden weitere klinische Studien durchgeführt. In diesen Fällen wird der Impfstoff bei Bedarf auch in bestimmten Risikogruppen getestet, um die Sicherheit weiter zu klären und die richtige Dosis für diese Personengruppe zu bestimmen.
Rennen nicht beendet
Es gibt immer noch mehr als 180 Covid-19-Impfstoffe im Rennen um die Welt. Dies ist wichtig, da möglicherweise mehr als ein Impfstoff benötigt wird, um den globalen Bedarf zu decken. Bestimmte Impfstoffe sind möglicherweise auch besser für Diabetiker, ältere Menschen oder Patienten mit HIV geeignet. Dazu müssen diese Impfstoffe jedoch auch in großen Phase-3-Studien mit Tausenden von Testpersonen nachgewiesen werden.
„Das Studiendesign kann dann vorsehen, dass der zu untersuchende Impfstoff einem Arm und dem bereits in der Kontrollgruppe registrierten Impfstoff verabreicht wird“, sagte Tanner. Auf diese Weise konnte festgestellt werden, ob der neue Impfstoff mindestens so wirksam und sicher ist wie der zugelassene.
Aber ist es ethisch vertretbar, der Kontrollgruppe einen zugelassenen Impfstoff vorzuenthalten? Vielleicht ja, wie amerikanische Forscher unter der Leitung von David Wendler in der Zeitschrift „Science“ geschrieben haben. Die Autoren ermutigen Wissenschaftler in laufenden Impfstoffstudien, gefährdete Personen auszuschließen, sammeln jedoch weiterhin wertvolle Daten von Teilnehmern, bei denen ein geringes Risiko für schwerwiegende krankheitsbedingte Schäden besteht.
Transparent kommunizieren
Das Wichtigste ist zunächst, dass genügend Menschen geimpft werden möchten. Sobald mindestens 60 bis 70 Prozent der Bevölkerung geimpft wurden, wird davon ausgegangen, dass die Herdenimmunität begonnen hat.
„Wir alle haben die Aufgabe, transparent, wissenschaftlich und ethisch über Impfstoffe zu kommunizieren“, sagte Tanner. „Wenn wir dies tun, steigt das Vertrauen in den Impfstoff und die Menschen werden auch geimpft“, sagte der Epidemiologe mit Überzeugung.

Hardcore-Musikfanatiker. Food-Evangelist. Freiberuflicher Spieler. Wannabe-Schriftsteller. Wegbereiter der Popkultur. Lebenslanger Unternehmer. Reise-Guru.
